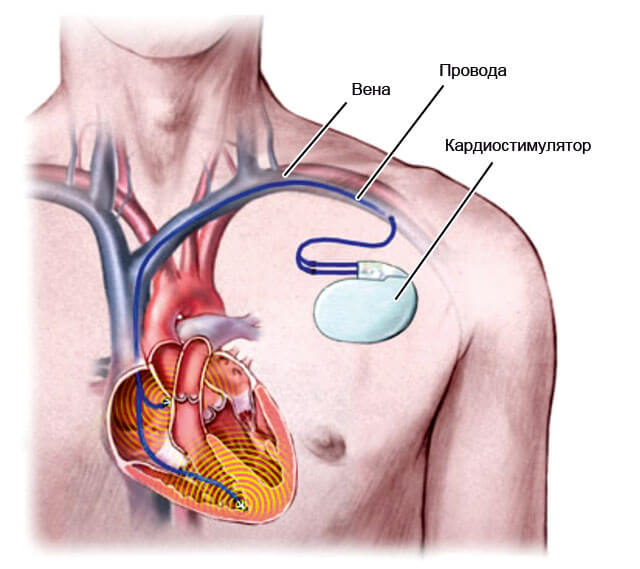
Дефект межжелудочковой перегородки: симптомы и хирургическое лечение
Содержание:
- Классификация
- Часто задаваемые вопросы
- Симптомы и внешние признаки
- Соответственно, дефекты межжелудочковой перегородки подразделяются на следующие виды:
- Причины
- Инфекционный эндокардит
- 9.8. ВРОЖДЁННЫЙ СТЕНОЗ УСТЬЯ АОРТЫ
- Диагностика при ДМЖП
- Причины ВПС
- Тетрада Фалло и беременность
- Правый желудочек
Классификация
В межжелудочковой перегородке выделяют 3 отдела: верхняя часть — мембранозная, прилегает к центральному фиброзному телу, средняя часть — мышечная, и нижняя — трабекулярная. Соответственно этим отделам называют и дефекты межжелудочковой перегородки, однако большинство из них имеют перимембранозную локализацию (до 80 %). На долю мышечных ДМЖП приходится 20 %.
По размерам дефекты подразделяют на большие, средние и малые. Для правильной оценки величины дефекта его размер надо сравнивать с диаметром аорты. Мелкие дефекты размером 1-2 мм, расположенные в мышечной части межжелудочковой перегородки, называются болезнью Толочинова-Роже. Вследствие хорошей аускультативной картины и отсутствия гемодинамических нарушений для их характеристики уместно выражение: «много шума из ничего». Отдельно выделяют множественные большие дефекты межжелудочковой перегородки, по типу «швейцарского сыра», имеющие неблагоприятное прогностическое значение.
Часто задаваемые вопросы
Сколько длится операция?
Чаще всего все манипуляции занимают от часа до трех. Длительность зависит от расположения дефекта, от сложности работы с контрольно-диагностическим оборудованием.
Какую анестезию применяют?
Для взрослых больных предпочтительнее местная анестезия. Благодаря применению современных препаратов и тому, что операция не предполагает травматических манипуляций, пациенты хорошо переносят вмешательство, находясь в сознании. Для детей и в редких случаях для взрослых возможно применение медикаментозного сна. Чувствуется только укол анестетика.
Как протекает послеоперационный период?
Если нет осложнений, то пациента отпускают домой через один-два дня. На месте прокола оставляют повязку для обеспечения стерильности. Часто назначают медикаментозные препараты, которые нужно принимать в течение первых месяцев после операции. В случае если пациент заболевает простудой – проводят профилактику приемом антибиотиков, чтобы избежать развития эндокардита.
Физические нагрузки требуется серьезно ограничить в первые месяцы. Но через полгода окклюдер покрывается собственными тканями, и риск осложнений снижается до минимума. Поэтому в первые шесть месяцев существуют рекомендации по отказу от вакцинации, от планирования беременности. А спустя полгода пациент может вести привычный для него образ жизни.
Симптомы и внешние признаки
- Мелкие дефекты – меньше 1/4 диаметра аорты или меньше 1 см. симптомы могут появиться и в 6 месяцев и во взрослом возрасте.
- Средние дефекты – меньше 1/2 диаметра аорты. Болезнь проявляется на 1-3 месяце жизни.
- Крупные дефекты – диаметр равен диаметру аорты. Болезнь проявляется с первых дней.
- Первая стадия – застой крови в сосудах. Накопление жидкости в ткани легких, частые бронхиты и пневмонии.
- Вторая стадия – спазмирование сосудов. Фаза временного улучшения, сосуды сужаются, но давление в них увеличивается 30 до 70 мм рт. ст. Считается лучшим периодом для операции.
- Третья стадия – склерозирование сосудов. Развивается, если вовремя не была проведена операция. Давление в правом желудочке и сосудах легких от 70 до 120 мм рт. ст.
Самочувствие ребенка
- синюшный оттенок кожи при рождении;
- одышка;
- малыш быстро утомляется и не может нормально сосать грудь;
- беспокойство и плаксивость из-за голода;
- нарушения сна;
- плохая прибавка в весе;
- ранние пневмонии, которые плохо поддаются лечению.
Объективные признаки
- возвышение грудной клетки в районе сердца – сердечный горб;
- во время сокращения желудочков (систолы) прощупывается дрожание, которое создает поток крови, проходя через отверстие в межжелудочковой перегородке;
- при прослушивании стетоскопом слышен шум, который вызван недостаточностью клапанов легочной артерии;
- в легких слышны свистящие хрипы и жесткое дыхание, связанные с выходом жидкости из сосудов в ткань легких;
- при простукивании выявляется увеличение размера сердца;
- увеличение печени и селезенки связанно с застоем крови в этих органах;
- в третей стадии характерно появление синеватого оттенка кожи (цианоза). Сначала на пальцах и вокруг рта, а потом по всему телу. Этот симптом появляется из-за того, что кровь недостаточно обогащается кислородом в легких и клетки тела испытывают кислородное голодание;
- на третьей стадии грудная клетка вздута, имеет вид бочки.
Соответственно, дефекты межжелудочковой перегородки подразделяются на следующие виды:
-
Наиболее распространенный вид дефектов. Локализован в мышечной части перегородки, окружающей мембранозную часть. Дефицит мышечной ткани может возникнуть в любом отделе, однако один из краев отверстия непременно образован соединительной тканью. Как правило, это часть перепончатого кольца аортального клапана. Эти дефекты могут образовываться в любой части перегородки.
-
Как следует из названия, в этом случае отверстие в межжелудочковой перегородке расположено под створками клапанов аорты и легочной артерии, в выходной части перегородки
-
Мышечные дефекты
Их края полностью состоят из мышечной ткани. Они могут образовываться в любой части перегородки, бывают множественными и/или сочетаются с перепончатыми дефектами
Что касается размеров дефекта межжелудочковой перегородки, то они измеряются по отношению к диаметру аорты. Если размер отверстия не превышает ¼ диаметра аорты, то такой дефект считается малым. При размерах, сопоставимых с половиной диаметра главного кровеносного сосуда, дефект относится к средним, а все, которые превышают этот размер, классифицируются как большие дефекты межжелудочковой перегородки. Естественно, что чем меньше отверстие, тем меньший вред наносится здоровью пациента.
Малые дефекты межжелудочковой перегородки, не превышающие 1 см в диаметре, имеют склонность к самостоятельному закрытию. Их доля в общем количестве дефектов межжелудочковой перегородки составляет 30-40%. Такие дефекты получили название болезнь Толочинова-Руже. У детей с малыми дефектами межжелудочковой перегородки уже на первой неделе жизни может выслушиваться грубый систолический шум. Тем не менее, физиологическое развитие таких детей протекает нормально. В старшем возрасте возможны жалобы на повышенную утомляемость при физических нагрузках.
На ЭКГ могут отсутствовать признаки патологии, или наблюдаться симптомы повышенной нагрузки на левый желудочек. В диагностических целях применяют ультразвуковое исследование, которое выявляет поток крови между желудочками. В сомнительных случаях или с целью уточнения диагноза проводят катетеризацию сердца, ангиографию.
При этом виде порока прогноз благоприятный. Иногда происходит самостоятельное закрытие дефекта, когда ребенок достигает возраста 4-5 лет. Такие пациенты должны находиться под наблюдением кардиолога. Хирургическое лечение в подобных случаях, как правило, не проводится.
Большие дефекты межжелудочковой перегородки могут создавать опасность для жизни ребенка уже в первые недели его жизни, поскольку развивается сердечная недостаточность: наблюдается отставание в развитии, возникают трудности при кормлении, нарушения сосательного рефлекса, одышка. Ребенок подвержен частым простудным заболеваниям со склонностью развития пневмонии. В области сердца при осмотре обнаруживается характерное выпячивание грудной клетки, при пальпации ощущается своеобразное дрожание во время систолы (сокращения сердечной мышцы). Постепенно одышка возникает и в покое, функциональные изменения легких ярко выражены, появляются нарушения работы печени, отеки на нижних конечностях.
Причины
- Инфекционные болезни матери в первые три месяца беременности: корь, краснуха, ветрянка.
- Употребление алкоголя и наркотических препаратов.
- Некоторые лекарственные средства: варфарин, препараты содержащие литий.
- Наследственная предрасположенность: порок сердца передается по наследству в 3-5% случаев.
- Множественные мелкие отверстия – самая легкая форма, которая мало влияет на состояние здоровья.
- Множественные крупные отверстия. Перегородка напоминает швейцарский сыр – самая тяжелая форма.
- Отверстия в нижней части перегородки, состоящей из мышц. Они чаще других затягиваются самостоятельно в течение первого года жизни ребенка. Этому способствует развитие мышечной стенки сердца.
- Отверстия, находящиеся под аортой.
- Дефекты в средней части перегородки.
Инфекционный эндокардит
Что такое инфекционный эндокардит?
Инфекционный эндокардит, или так называемый бактериальный эндокардит – это воспаление внутренней оболочки сердца. Заболевание вызванное, как правило, бактериями, которые с током крови попадают в сердце и вызывают серьезные изменения клапанов и других структур сердца. Заболевание это довольно редкое. Существует категория пациентов склонных к развитию инфекционного эндокардита
Таким пациентам крайне важно проводить профилактику инфекционного эндокардита
Какие симптомы должны насторожить?
Необъяснимая длительно существующая, часто не высокая (37,5 °C) температура, бледность кожи, потеря в весе, излишняя потливость.
Кому необходимо проводить антибиотикопрофилактику инфекционного эндокардита?
- Всем пациентам с неоперированными врожденными пороками сердца за исключением вторичного дефекта межпредсердной перегородки, не нуждающихся в коррекции маленьких дефектов межжелудочковой перегородки (менее 2 мм) и маленьких боталловых протоков (менее 2 мм).
- Всем пациентам после радикальной хирургической коррекции врожденных пороков сердца с искусственными сосудистыми или клапанными протезами и синтетическими заплатами (кондуитами, в некоторых случаях коарктацией аорты) на протяжении 6 месяцев после операции.
- Всем пациентам после паллиативного хирургического лечения врожденных пороков сердца (анастомоз Блелока, суживания легочной артерии).
- Пациентам после эндоваскулярных вмешательств (включая диагностическую катетеризацию полостей сердца) на протяжении 6 месяцев после вмешательства.
Все выше перечисленные категории пациентов являются пациентами группы риска по развитию инфекционного эндокардита.
Когда проводится профилактика инфекционного эндокардита?
- Стоматологические процедуры с риском кровотечения (кроме стоматологических процедур на молочных зубах).
- Все хирургические и эндоскопические процедуры с риском повреждения слизистых оболочек и кровотечения (например, тонзилэктомия — удаление миндалин, аденэктомия, бронхоскопия с биопсией).
- Не проводится профилактика инфекционного эндокардита перед родоразрешением естественным путем.
Как проводится профилактика инфекционного эндокардита?
Профилактика инфекционного эндокардита проводится пациентам группы риска за 30-60 минут до предполагаемой процедуры с риском кровотечения путем однократного назначения антибиотиков перорально (через рот):
- Амоксициллин, Амоксиклав, Аугментин, Уназин 50мг/кг (максимально 2 г.)
- При аллергии к ампицилину — Клиндамицин 20 мг/кг
При невозможности перорального приема те же дозы вводятся внутривенно.
Нецелесообразно проводить антибиотикопрофилактику инфекционного эндокардита при наличии вирусной инфекции (ОРВИ). Подъем температуры выше, чем 38,5 °C, которая держится более 2-х дней, следует расценивать как присоединение бактериальной инфекции. В данном случае необходимо назначение антибиотиков курсом на 5 — 7 дней. Антибиотики назначаются участковыми врачами по месту жительства.
Так как наиболее частой причиной возникновения инфекционного эндокардита являются микроорганизмы, живущие в полости рта и носоглотки, тщательная гигиена ротовой полости является обязательной (чистка зубов не менее 2-х раз в день).
Вакцинация
Вакцинация является своеобразной профилактикой инфекционного эндокардита вирусного происхождения. Всем детям с врожденными пороками сердца, входящих в группу риска по возникновению инфекционного эндокардита показана плановая вакцинация согласно календарю прививок. Кроме того рекомендуется проходить ежегодную противогриппозную вакцинацию. Наиболее оптимальный период проведения противогриппозной вакцинации сентябрь-ноябрь всем пациентам группы риска старше 6 месяцев. Рекомендуется не проводить вакцинацию за 14 дней до кардиохирургического вмешательства и 14 дней после кардиохирургического вмешательства.
Если у Вас остались вопросы звоните — 044 2756148, пишите — occluder.com.ua@gmail.com или спрашивайте на сайте — occluder.com.ua.
Ящук Н.С.
Инфекционный эндокардит (скачать)
Инфекционный эндокардит (PDF)
Важная информация для пациентов
Мы специализируемся на лечении сердца современным методом с применением лучших технологий
Посмотрите, чем мы
можем вам помочь
Более 300 имплантаций окклюдеров, стентов и спиралей ежегодно
Наибольшее количество операций среди кардиоцентров Украины
9.8. ВРОЖДЁННЫЙ СТЕНОЗ УСТЬЯ АОРТЫ
Врождённый стеноз устья аорты — сужение выносящего тракта левого желудочка в области аортального клапана. В зависимости от уровня расположения обструкции стеноз может быть клапанным, подклапанным, надклапанным.
Распространённость
Врождённый стеноз устья аорты составляет 6% от всех врождённых пороков сердца. Наиболее часто отмечают клапанный стеноз (80%), реже подклапанный и надклапанный. У мужчин стеноз устья аорты наблюдают в 4 раза чаще, чем у женщин.
ГЕМОДИНАМИКА
• Клапанный стеноз (см. рис. 9-7). Наиболее часто аортальный клапан двустворчатый, при этом отверстие расположено эксцентрично. Иногда клапан состоит из одной створки. Реже клапан состоит из трёх створок, сращённых между собой одной или двумя спайками.
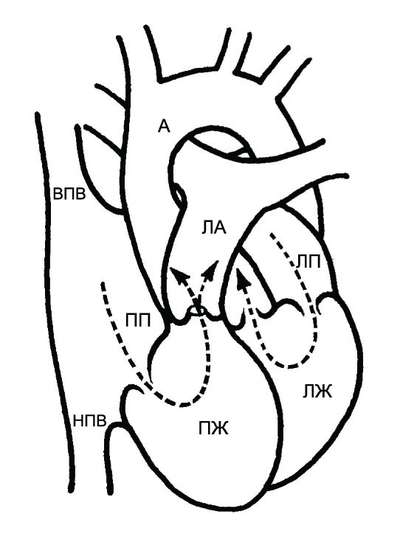 Рис. 9-7. Гемодинамика при стенозе устья лёгочной артерии. А — аорта; ЛА — лёгочная артерия; ЛП — левое предсердие; ЛЖ — левый желудочек; ПП — правое предсердие; ПЖ — правый желудочек; НПВ — нижняя полая вена; ВПВ — верхняя полая вена.
Рис. 9-7. Гемодинамика при стенозе устья лёгочной артерии. А — аорта; ЛА — лёгочная артерия; ЛП — левое предсердие; ЛЖ — левый желудочек; ПП — правое предсердие; ПЖ — правый желудочек; НПВ — нижняя полая вена; ВПВ — верхняя полая вена.
• При подклапанном стенозе отмечают три вида изменений: дискретную мембрану под аортальными створками, туннель, мышечное сужение (субаортальная гипертрофическая кардиомиопатия, см. главу 12 «Кардиомиопатии и миокардиты»).
• Надклапанный стеноз устья аорты может быть в виде мембраны или гипоплазии восходящей части аорты. Признаком гипоплазии восходящей аорты считают отношение диаметра дуги аорты к диаметру восходящей аорты менее 0,7. Нередко надклапанный стеноз устья аорты сочетается со стенозом ветвей лёгочной артерии.
Надклапанный стеноз устья аорты в сочетании с умственной отсталостью называется синдромом Уильямса.
Стеноз устья аорты часто сочетается с другими врождёнными пороками сердца — ДМЖП, ДМПП, открытым артериальным протоком, коарктацией аорты.
В любом случае создаётся препятствие кровотоку и развиваются изменения, приведённые в главе 8 «Приобретённые пороки сердца». Со временем развивается кальцификация клапана. Характерно развитие постстенотического расширения аорты.
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Жалобы
Большинство больных при незначительном стенозе жалоб не предъявляют. Появление жалоб свидетельствует о выраженном стенозе устья аорты. Возникают жалобы на одышку при физической нагрузке, быструю утомляемость (из-за сниженного сердечного выброса), обмороки (в результате гипоперфузии мозга), загрудинные боли при физической нагрузке (из-за гипоперфузии миокарда). Возможно возникновение внезапной сердечной смерти, но в большинстве случаев этому предшествуют жалобы или изменения на ЭКГ.
Осмотр, перкуссия
См. раздел «Стеноз устья аорты» в главе 8 «Приобретённые пороки сердца».
Пальпация
Определяют систолическое дрожание вдоль правого края верхней части грудины и над сонными артериями. При пиковом систолическом градиенте давления менее 30 мм рт.ст. (по данным ЭхоКГ) дрожание не выявляется. Низкое пульсовое давление (менее 20 мм рт.ст.) свидетельствует о значительной выраженности стеноза устья аорты. При клапанном стенозе обнаруживают малый медленный пульс.
Аускультация сердца
Характерно ослабление II тона или его полное исчезновение вследствие ослабления (исчезновения) аортального компонента. При надклапанном стенозе устья аорты II тон сохранён. При клапанном стенозе устья аорты выслушивают ранний систолический клик на верхушке сердца, отсутствующий при над- и подклапанных стенозах. Он исчезает при выраженном клапанном стенозе устья аорты.
Диагностика при ДМЖП
Диагностические ультразвуковые исследования выявляют ДМЖП еще на этапе внутриутробного развития. С их помощью также подтверждают и уточняют диагноз после рождения ребенка. При необходимости могут дополнительно назначаться инвазивные методы обследования, невозможные во время внутриутробного развития. Помимо осмотра врача проводится:
электрокардиография. Результат может быть как нормальным, так и с признаками перегрузки правых отделов сердца. Иногда при их перерастяжении страдает проводящая система, в итоге развивается аритмия, и это тоже отражается на ЭКГ
эхокардиография позволяет оценить размеры ДМЖП, особенности кровотока в полостях сердца и состояние всех его отделов
цветное дуплексное сканирование необходимо для уточнения результатов, полученных ранее, определения местоположения дефекта на перегородке
Это важно для выбора техники закрытия дефекта и используемых при этом материалов
зондирование сердца с помощью введенного через периферические сосуды катетера назначается, если после других методов исследования остались неясные вопросы
Необходимость в проведении всех этих методов возникает далеко не всегда. Опытные специалисты часто получают все нужные данные уже после нескольких диагностических тестов.
По результатам обследования может быть принято решение о хирургическом лечении, если:
- ДМЖП слишком велик, имеются и быстро нарастают признаки сердечной недостаточности. Промедление в таких случаях слишком опасно
- по мере наблюдения ребенка ДМЖП не уменьшается
Как правило, хирургическое лечение ДМЖП проводится одномоментно и состоит в ликвидации патологического сообщения между желудочками. Однако иногда ребенок находится в тяжелом состоянии, и радикальная операция для него слишком рискованна. Тогда ему назначают консервативную терапию для борьбы с сердечной недостаточностью и «разгрузки» правых отделов сердца. И на этом фоне в качестве первого этапа хирургического лечения неплотно перевязывают ствол легочной артерии, суживая ее просвет. В течение нескольких месяцев это позволяет преодолевать повышение давления в малом круге кровообращения. Состояние ребенка улучшается, и на втором этапе выполняют радикальную операцию.
Современный подход к хирургическому лечению дефекта межжелудочковой перегородки подразумевает радикальное устранение отверстия между желудочками в ходе традиционной открытой операции с аппаратом искусственного кровообращения, рентгенхирургического малоинвазивного внутрисосудистого вмешательства или гибридной операции, включающей элементы двух первых.
Причины ВПС
В качестве основных ведущих причины в формировании пороков, чаще всего, выступают структурные и количественные хромосомные аномалии, и мутации, т.е. первичные генетические факторы.
Также необходимо уделять внимание потенциально тератогенным факторам внешней среды: различные внутриутробные инфекции (вирусы краснухи, цитомегаловирус, коксаки, инфекционные заболевания у матери в первом триместре), лекарственные препараты (витамин А, противоэпилептические средства, сульфазалазин, триметоприм), постоянный контакт с токсичными веществами (краски, лаки). Кроме того, нужно помнить, что отрицательное влияние на внутриутробное развитие оказывают как материнские факторы: предшествующие данной беременности репродуктивные проблемы, наличие сахарного диабета, фенилкетонурии, алкоголизма, курение, возраст, но также, и факторы со стороны отца – возраст, употребление наркотических средств (кокаин, марихуана).. Ведущая роль принадлежит мультифакториальной теории развития врожденных пороков сердца (до 90%).
Ведущая роль принадлежит мультифакториальной теории развития врожденных пороков сердца (до 90%).
Виды врожденных пороков сердца
-
Дефект межпредсердной перегородки (ДМПП) или открытое овальное окно – диагностируется при выявлении одного либо нескольких отверстий в межпредсердной перегородке. Один из часто встречающихся врожденных пороков сердца. В зависимости от расположения дефекта, его величины, силы тока крови определяются более или менее выраженные клинические признаки. Часто ДМПП сочетается с другими аномалиями сердца и определяться при синдроме Дауна.
-
Дефект межжелудочковой перегородки (ДМЖП) – диагностируется при недоразвитии межжелудочковой перегородки на различных уровнях с формированием патологического сообщения между левым и правым желудочками. Может встречаться как изолированно, так и вместе с другими аномалиями развития. При малом дефекте – чаще нет выраженного отставания в физическом развитии. ДМЖП опасен тем, что может приводить к развитию легочной гипертензии, и потому, должен своевременно корректироваться оперативным путем.
-
Коартация аорты – сегментарное сужение просвета аорты с нарушением нормального кровотока из левого желудочка в большой круг кровообращения. Выявляется до 8% всех случаев ВПС, чаще у мальчиков, нередко сочетается с другими аномалиями.
-
Открытый артериальный проток – диагностируется при не заращении Баталлова протока, определяемого у новорожденных и зарастающего в последующем. В результате, происходит частичный сброс артериальной кровь из аорты в легочную артерию. При данном ВПС чаще не бывает тяжелых клинических проявлений, однако, патология требует хирургической коррекции, поскольку сопряжена с высоким риском внезапной сердечной смерти.
-
Атрезия легочной артерии – диагностируется недоразвитие (полное либо частичное) створок клапана легочной артерии с развитием обратного заброса крови из легочной артерии в полость правого желудочка. В последующем приводит к недостаточному кровоснабжению легких.
-
Стеноз клапана легочной артерии – аномалия, при которой диагностируют сужение отверстия клапана легочной артерии. В результате патологии, чаще всего, створок клапана, нарушается нормальный кровоток из правого желудочка в легочный ствол.
-
Тетрада Фалло – сложный сочетанный ВПС. Объединяет дефект межжелудочковой перегородки, стеноз легочной артерии, гипертрофию правого желудочка, декстрапозицию аорты. При данной патологии происходит смешение артериальной и венозной крови.
-
Транспозиция магистральных сосудов – также сложный ВПС. При данной патологии аорта отходит от правого желудочка и несет венозную кровь, а легочный ствол отходит от левого желудочка и несет артериальную кровь, соответственно. Парок протекает тяжело, сопряжен с высокой летальностью новорожденных.
-
Декстрокардия – аномалия внутриутробного развития, арактеризующаяся правосторонним размещением сердца. Зачастую, наблюдается «зеркальное» расположениее других непарных внутренних органов.
-
Аномалия Эбштейна – редко встречающийся врожденный порок сердца, диагностируется при изменении месторасположения створок трехстворчатого клапана. В норме — от предсердно-желудочкового фиброзного кольца, при аномалии — от стенок правого желудочка. Правый желудочек имеет меньшие размеры, а правое предсердие удлинено, вплоть до аномальных клапанов.
Тетрада Фалло и беременность
ОПИСАНИЕ
Тетрада Фалло – это врожденный порок сердца представленный дефектом межжелудочковой перегородки, аортой «наездником» (декстрапозиция), стенозом легочной артерии и гипертрофией миокарда правого желудочка. Тетрада Фалло относится к наиболее распространенным порокам сердца синего типа, встречается в 10 -12% от всех врожденных пороков сердца. Частота порока сердца у потомства составляет примерно 5%.
ПРИЧИНЫ
Основной причиной развития заболевания служит нарушение генома. Генетики относят его к понятию синдром diGeorge (Диджорджи или Ди Георге).
Причина развития синдрома кроется в субмикроскопической делеции (отщеплении) района q11.2 хромосомы 22. Сокращенно этот вариант патологии генетики пишут так: «del 22 q11.2». Но интересно то, что подобное нарушение генотипа проявляется не только патологией развития сердца в виде тетрады Фалло. Делеция этого участка имеет также обозначения DGCR (DiGeorge syndrome critical region) и VCF(velocardiofacial syndrome).
На уровне организма при этом встречаются проявления со стороны различных органов и систем. Обычно синдром сочетает гипокальциемию (за счет недоразвития паращитовидных желез), Т-клеточный иммунодефицит (из-за недоразвития тимуса), пороки выходных отверстий сердца (к которым относят и тетраду Фалло), а также лицевые мальформации. В связи с тем, что тетрада Фалло является лишь одним из вариантов пороков, связанных с «del 22», вполне резонно предположить, что данный генетический дефект встречается не реже, чем тетрада Фалло. И действительно, синдром diGeorge встречается примерно у одного из 3000 новорождённых.
СИМПТОМЫ
Цианоз – основной симптом тетрады Фалло. Степень цианоза и время его появления зависит от выраженности стеноза лёгочной артерии. В основном, цианоз развивается к 3 месяцам, к 1 году.
Цианоз нарастает с ростом активности ребенка. Постоянным признаком порока является одышка, которая резко возрастает при малейшей физической нагрузке. В тяжелых случаях при тетраде Фалло, развиваются приступы удушья. Возникают они, как правило, в возрасте от 6 до 24 месяцев. Ребенок становится беспокойным, выражение лица испуганное, зрачки расширены, одышка и цианоз нарастают, конечности холодные; затем следует потеря сознания, судороги и возможно развитие комы и летальный исход.
Приступы длятся обычно несколько минут. Постепенно развивается задержка физического развития, пациенты часто имеют пальцы рук и ног в виде «барабанных палочек». Практически с рождения выслушивается грубый систолический шум вдоль левого края грудины.
Осложнения при беременности
До беременности рекомендуется хирургическое лечение порока сердца. Пациенты с полной коррекцией порока и отсутствием сердечной недостаточности беременность переносят хорошо, хотя в некоторых случаях могут иметь место нетяжелые нарушения ритма сердца. При некоррегированном пороке имеется высокий риск материнской смертности, невынашивания беременности и внутриутробной задержки роста плода. При некоррегированном пороке беременность противопоказана.
Факторы риска неблагоприятного исхода беременности:
- высокий гематокрит, превышающий 65%;
- застойная сердечная недостаточность;
- увеличение размеров сердца;
- насыщение крови кислородом менее 80%.
ЛЕЧЕНИЕ
Выделяют радикальные и паллиативные способы коррекции порока.Радикальная ликвидация порока проводится в условиях кардиоплегии и искусственного кровообращения. Операция заключается в закрытии межжелудочкового дефекта и ликвидации стеноза.
Паллиативные операции содержатся в наложении окольных межартериальных анастомозов. Задача операции — предоставить детям шанс пережить тяжелый период, для того, чтобы потом провести радикальную операцию.
Правый желудочек
Функциональная анатомия правого желудочка
Объем правого желудочка у новорожденных составляет 8,5-11 см3,
у детей первого года жизни — 13-20 см3, в 7-9 лет — 28-40 см3,
к 18 годам достигает 150-225 см3. У новорожденных и детей до
1 года длина правого желудочка составляет 4,3-6,2 см, ширина 2,1-3,2
см, у 7-12 летних детей длина желудочка увеличивается до 5-7,2 см,
ширина — до 2-3,5 см. К 18 годам длина правого желудочка достигает
7,3-9,2 см, ширина — 3-5 см. Толщина свободной стенки правого желудочка
у детей до 1 года равна 0,1-0,16 см, к 6 годам она возрастает до 0,2
см, а к 12 годам достигает 0,32 см. Полость правого желудочка имеет
выраженную трабекулярность, при этом основания сосочковых мышц располагаются
в толще трабекул.
Одномерная эхокардиография правого желудочка
Приточный отдел правого желудочка изучают в I стандартной позиции,
отточный в IV позиции. Поперечный размер правого желудочка по данным
эхометрии не соответствует анатомическому поскольку ультразвуковой
луч пересекает полость желудочка в зоне соответствующей 1/3 максимального
поперечного диаметра сферы. Толщина свободной стенки правого желудочка
в одномерном и двухмерном изображении обычно больше, чем анатомическая
из-за выраженной трабекулярности полости. Нормальные значения полости
правого желудочка и толщины его свободной стенки представлены в таблицах
5, 8, 15.
Семиотика правого желудочка
Дилатация правого желудочка
- Идиопатическая дилатация легочной артерии.
- Врожденное отсутствие клапана легочной артерии.
- Частичное отсутствие перикарда.
- Дефект межпредсердной перегородки (первичный, вторичный).
- Аномальный дренаж легочных вен (частичный, тотальный).
- Аномалия Эбштейна (имеется в виду увеличение атриализированной
порции желудочка). - Недостаточность трикуспидального клапана.
- Недостаточность клапана легочной артерии.
- Фистула правой коронарной артерии в правый желудочек.
- Врожденное отсутствие клапана легочной артерии.
- Опухоль правого желудочка.
- Синдром гипоплазии левого желудочка.
- Транспозиция магистральных сосудов.
- Легочная гипертензия (первичная, вторичная).
- Миокардит.
- Застойная сердечная недостаточность.
- Рестриктивная кардиомиопатия.
- Изменение позиции сердца (ротация правого желудочка
кпереди).
Уменьшение полости правого желудочка
- Атрезия трикуспидального клапана.
- Тампонада перикарда.
- Атрезия легочной артерии с интактной межжелудочковой
перегородкой. - Концентрическая гипертрофия правого желудочка.
- Аневризма межжелудочковой перегородки.
- Сдавление правого желудочка объемным образованием
средостения. - Изменение позиции сердца (ротация правого желудочка
кзади).
Гипертрофия свободной стенки правого желудочка
(увеличение толщины стенки более 3 — 5 мм)
- Стеноз легочной артерии (инфундибулярный, клапанный,
надклапанный, стеноз левой или правой ветви легочной артерии). - Легочная гипертензия (первичная, вторичная).
- Рестриктивная кардиомиопатия.
- Опухоль правого желудочка.
- Тетрада Фалло.
- Транспозиция магистральных сосудов.
- У новорожденных, рожденных от матерей,страдающих
диабетом. - Гипертрофическая кардиомиопатия с обструкцией выходного
тракта правого желудочка.
Дополнительные эхосигналы в полости правого желудочка
- Аномальные мышечные пучки.
- Опухоли правого желудочка (чаще рабдомиомы).
- Разрыв аневризмы синуса Вальсальвы в полость правого
желудочка. - Аневризма межжелудочковой перегородки.
- Тромб в правом желудочке.
Двухмерная эхокардиография правого желудочка
Правый желудочек визуализируют во взаимно перпендикулярных осях сканирования:
приточную порцию — в проекции 4-х камер с верхушки и поперечном парастернальном
сечении; отточную — в парастернальной проекции выходного тракта
правого желудочка и поперечном сечении на уровне магистральных сосудов.
Объемная перегрузка правого желудочка
- Дилатация правого желудочка.
- Парадоксальное движение межжелудочковой перегородки
(см) (при наличии легочной гипертензии может не определяться). - Увеличение экскурсии передней створки трикуспидального
клапана. - Систолическое трепетание трикуспидального клапана.
- Уменьшение амплитуды и скорости открытия передней
створки митрального клапана.
Гипертрофия правого желудочка
- Увеличение толщины свободной стенки правого желудочка
более 5 мм. - Гипертрофия (правосторонняя) межжелудочковой перегородки.
- Повышенная трабекулярность полости правого желудочка.